Doctor Endoscopy
👨⚕️Щербаченя Никита Александрович
🔬Знаю всё о вашем внутреннем мире🫁🫀
✅Врач-эндоскопист🔬
✅Врач-хирург.
✅Врач-онколог.
✅Все виды эндоскопии экспертного уровня.
✅Веду канал о доказательной эндоскопии, медицине и немного о себе 🩺 Связанные каналы | Похожие каналы
7 368
подписчиков
Популярное в канале
✅Микроскопический колит ☑️Хроническое заболевание толстой кишки, которое описывается клинико-па...
Юмористический пост🙂 🎯Смотрю, как врач не выполнил инверсию в желудке. 🎯Смотрю, как врач не осмо...
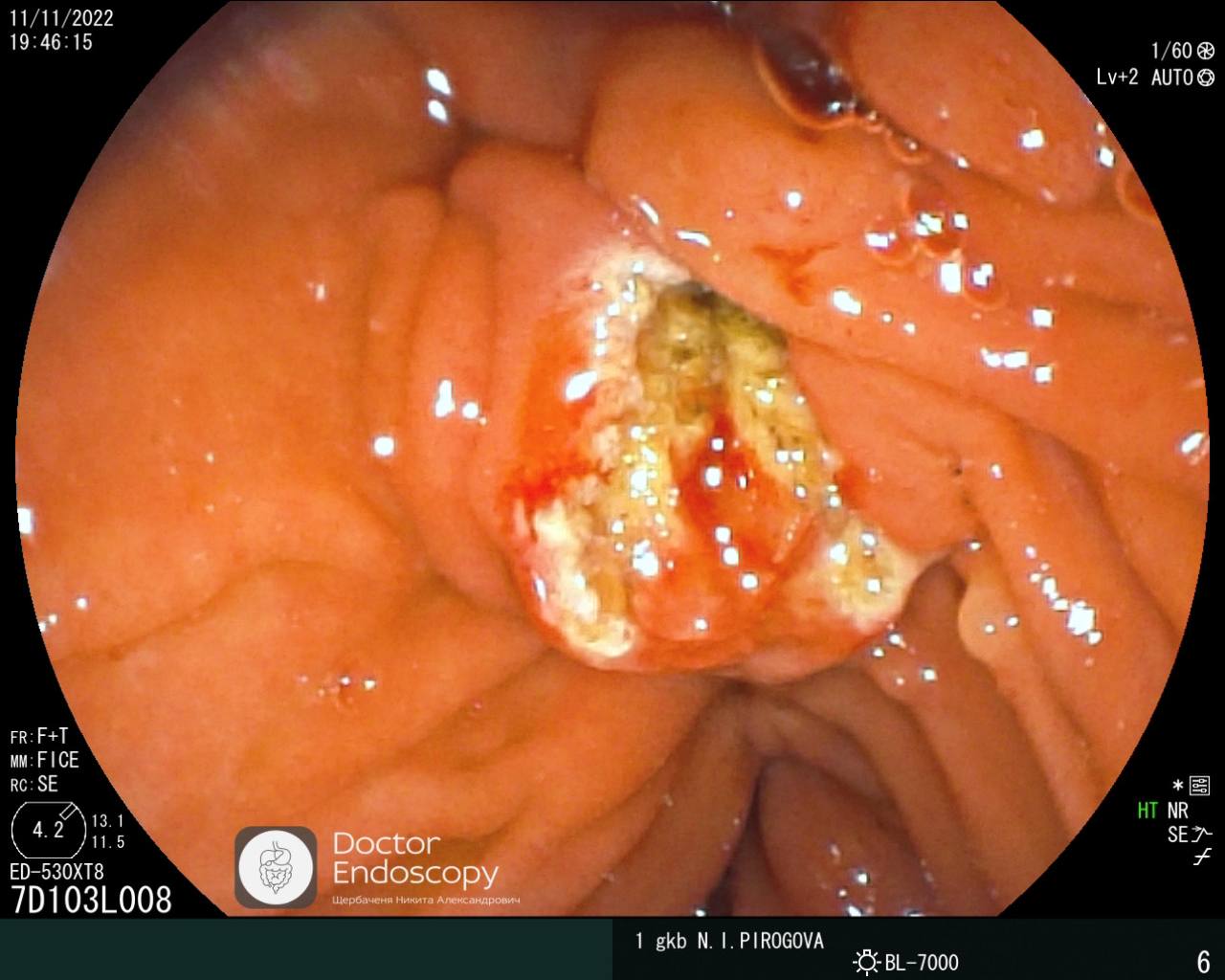
☑️Редкая причина механической желтухи. ☑️Печёночный сосальщик (печёночная двуустка)-вид плоских ...
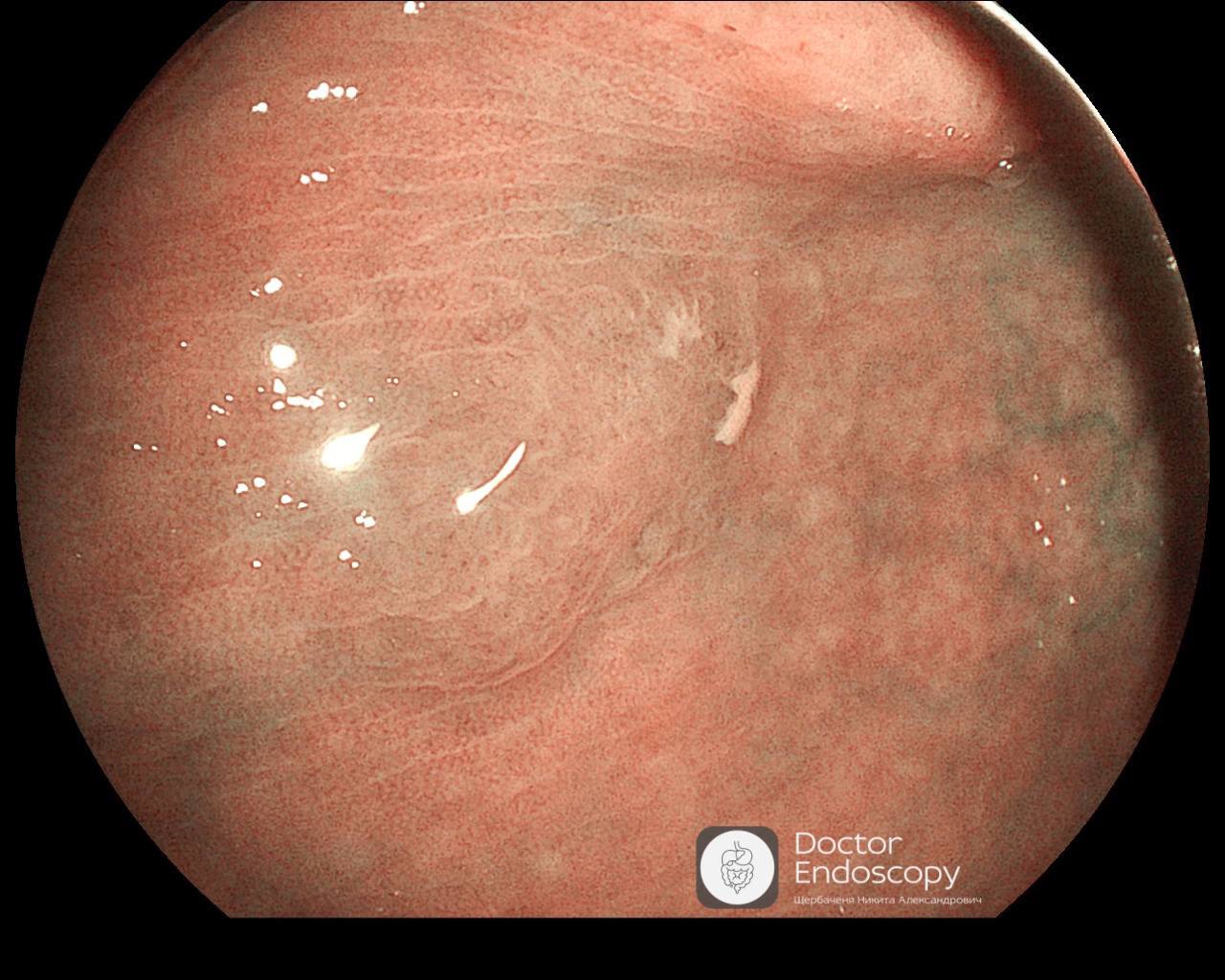
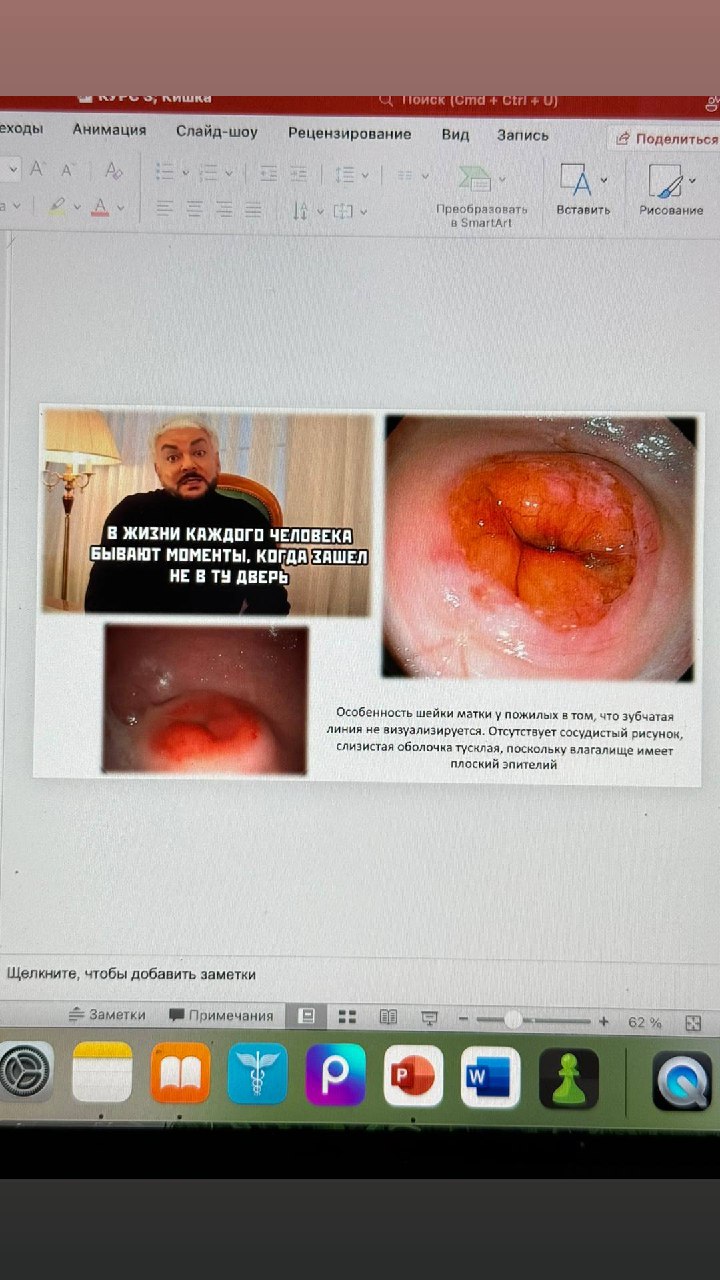
🦷 Коварное зубчатое образование 📌Ко мне на приём пришла молодая девушка с жалобами на периодиче...
Доброе утро ☀️ Небольшой кейс про вчерашнее удаление образования на ножке. ☑️На фото 1-2 мы вид...