RUSSCO - Российское общество клинической онкологии
Российское общестов клинической онкологии Связанные каналы | Похожие каналы
3 386
подписчиков
Популярное в канале
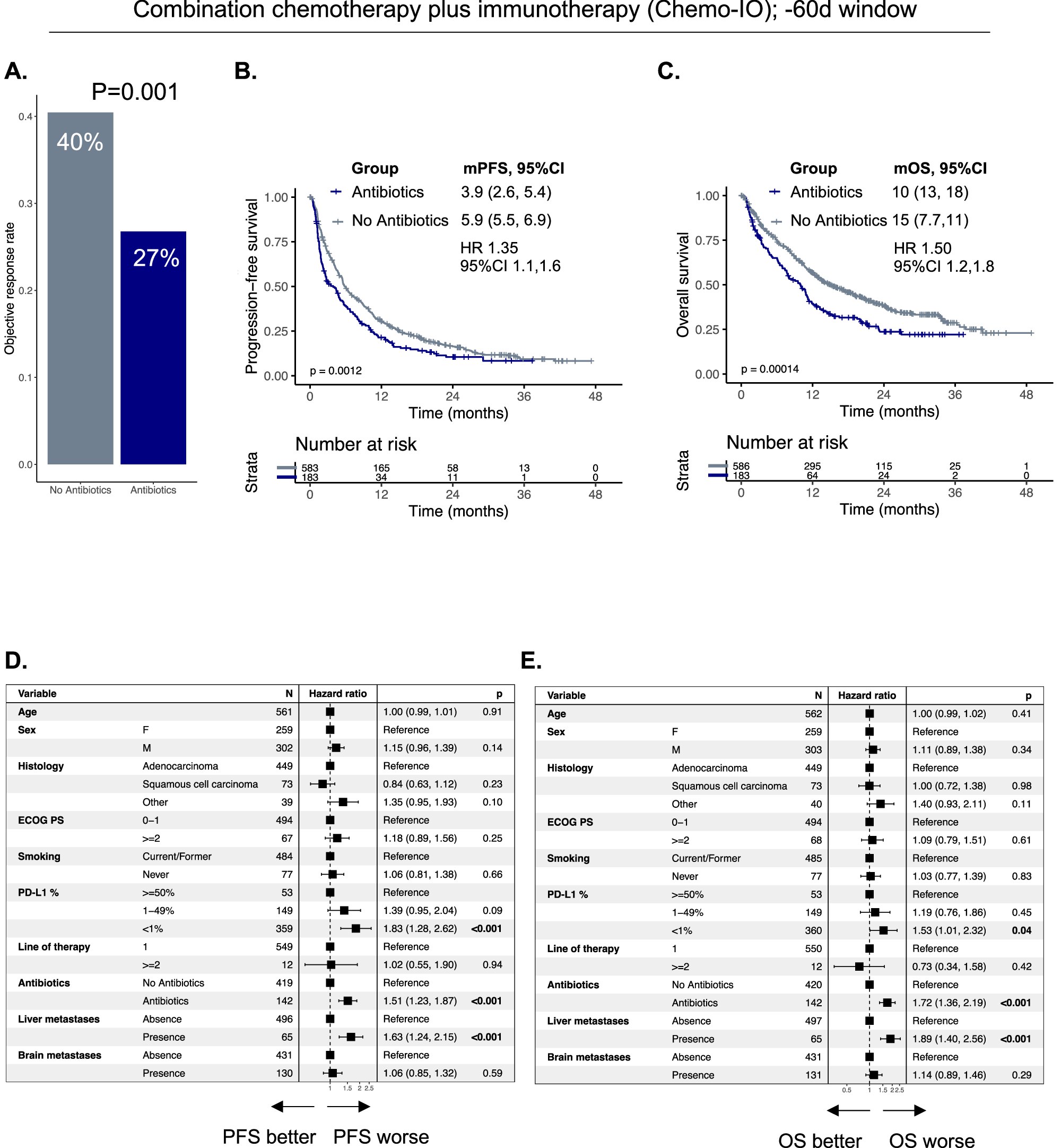
Антибиотики ухудшают показатели выживаемости у пациентов с НМРЛ до и во время химио-иммунотерапии...

«Алексей Трякин: российская фарминдустрия не может конкурировать с западной на равных» (интервью ...

RUSSCO рекомендует Уважаемые коллеги! Российское общество клинической онкологии (RUSSCO) провело ...
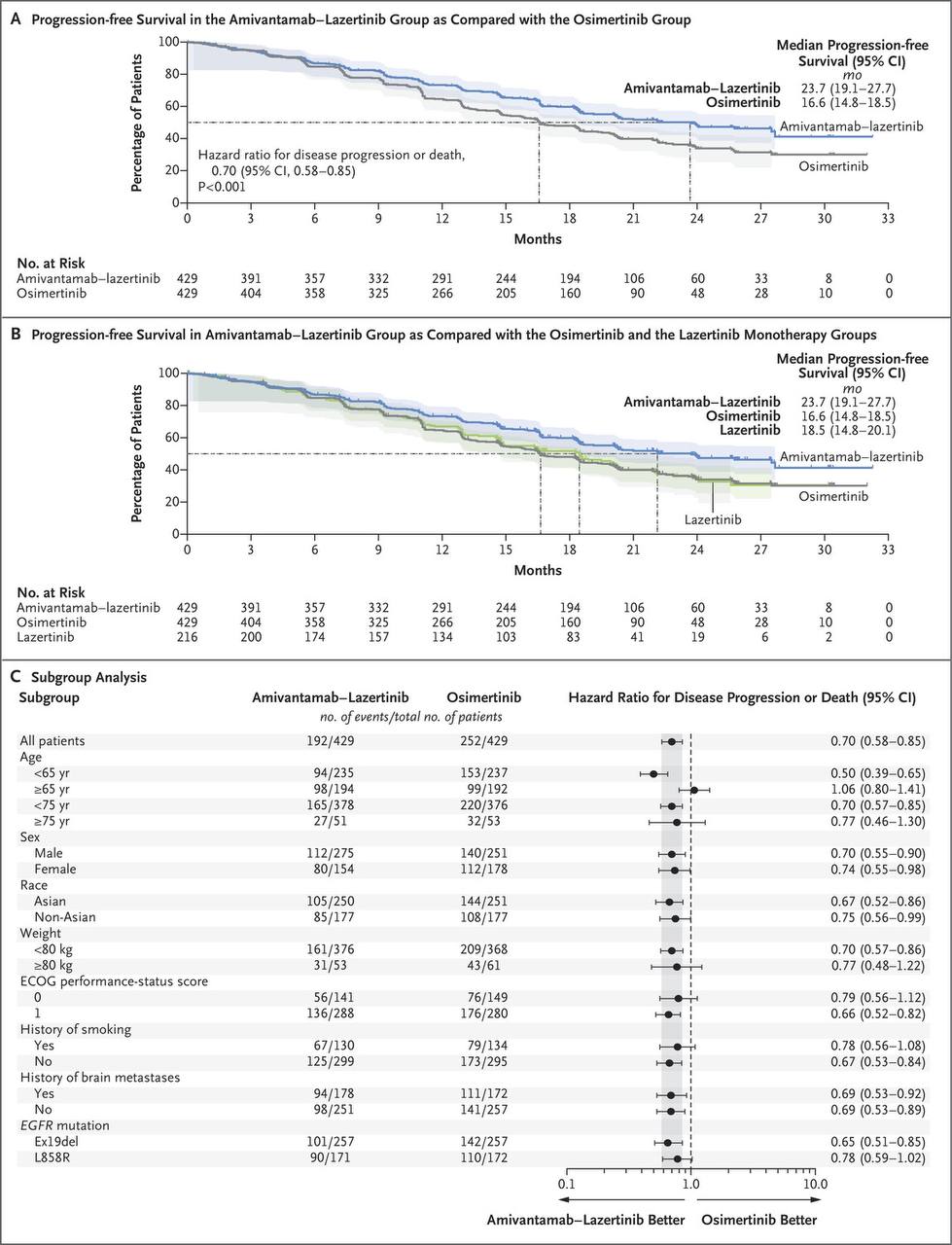
MARIPOSA trial: комбинация амивантамаба и лазертиниба демонстрирует преимущество ВБП над осимерти...

НЕ ПРОПУСТИТЕ! Уважаемые коллеги! Российское общество клинической онкологии (RUSSCO) провело 7-8 ...


